为贯彻落实《中华人民共和国标准化法》《中华人民共和国疫苗管理法》和《关于促进团体标准规范优质发展的意见》等法律法规及相关政策,根据《中国疫苗行业协会团体标准管理办法》《中国疫苗行业协会标准立项评审细则》和协会标准化工作委员会2024年度标准化工作计划,为有力推动新产品、新业态、新模式发展,促进疫苗行业高质量产品与服务供给,中国疫苗行业协会于3月9日在北京举办2024年度标准立项评审会。中国疫苗行业协会副会长李向明、国家卫生健康委员会法规司一级巡视员陈宁姗、中国标准化协会理事长于欣丽出席会议并致辞,中国疫苗行业协会标准化工作委员会主任委员雷苏文研究员主持会议。
会上,国家卫生健康委陈宁姗一级巡视员高度肯定了中国疫苗行业协会的标准化工作,陈巡表示,标准化工作发展与创新,是法制化、规范化的一个重要方面,这项关系到民生福祉的工作一直得到国家卫生健康标准委员会和中国疫苗行业协会的大力支持,并祝愿协会团体标准化工作发展成为疫苗领域更高更好的新平台。中国标准化协会于欣丽理事长在致辞中鼓励各申报团队利用好中国疫苗行业协会的平台,将优质资源进行交流整合,推动疫苗行业创新发展,并强调了本次标准立项评审工作的重要性,要求以“高质量标准”为今后疫苗行业的发展提供强有力的技术支撑。李向明副会长对各位评审专家及项目申报团队的积极参与和大力支持表示感谢,高度肯定了标准化工作委员会既往的工作,推动了疫苗行业标准化工作的稳步发展。会上推举中国医学科学院北京协和医学院群医学及公共卫生学院执行院长、中华预防医学会副会长杨维中研究员为专家组总组长兼第一组专家组组长,江苏省疾控中心副主任朱凤才研究员为第二组专家组组长、中国疾控中心实验室管理处副处长魏强研究员为第三组组长。标准化工作委员会孙乃玲秘书长对本次立项评审的依据、评审细则和要点进行讲解。 自中国疫苗行业协会发布《中国疫苗行业协会关于征集2023年度标准项目的通知》以来,科研机构、大专院校、学协会、企业等多家单位及组织申报了60项标准项目,经中国疫苗行业协会组织专家进行合规性审查,通过合规性审查33项,其中30个项目参加本次立项评审,是自标准化工作委员会成立以来,参与领域最多,覆盖门类最广,标准数量最多的一次评审。本次立项评审会审查采用专家组分组评议的方式,由标准申报团队向专家组汇报立项背景、标准的科学性、规范性、时效性等相关技术内容,专家组对各项目进行了质询和评审,经过认真讨论和评估,全体专家合议并投票产生最终结果。经评审,共有21个标准项目通过立项评审(清单详见附件)。 下一步,中国疫苗行业协会将继续以标准为载体推动疫苗行业自律、建立健全行业规范,以高质量标准化平台衔接行业内专家与企业多方合作,推动疫苗行业高标准建设、高质量发展,保证团体标准的生命力。

大会现场

主席台

李向明副会长致辞 陈宁姗一级巡视员致辞 于欣丽理事长致辞

杨维中院长主持立项评审 雷苏文主任委员主持会议
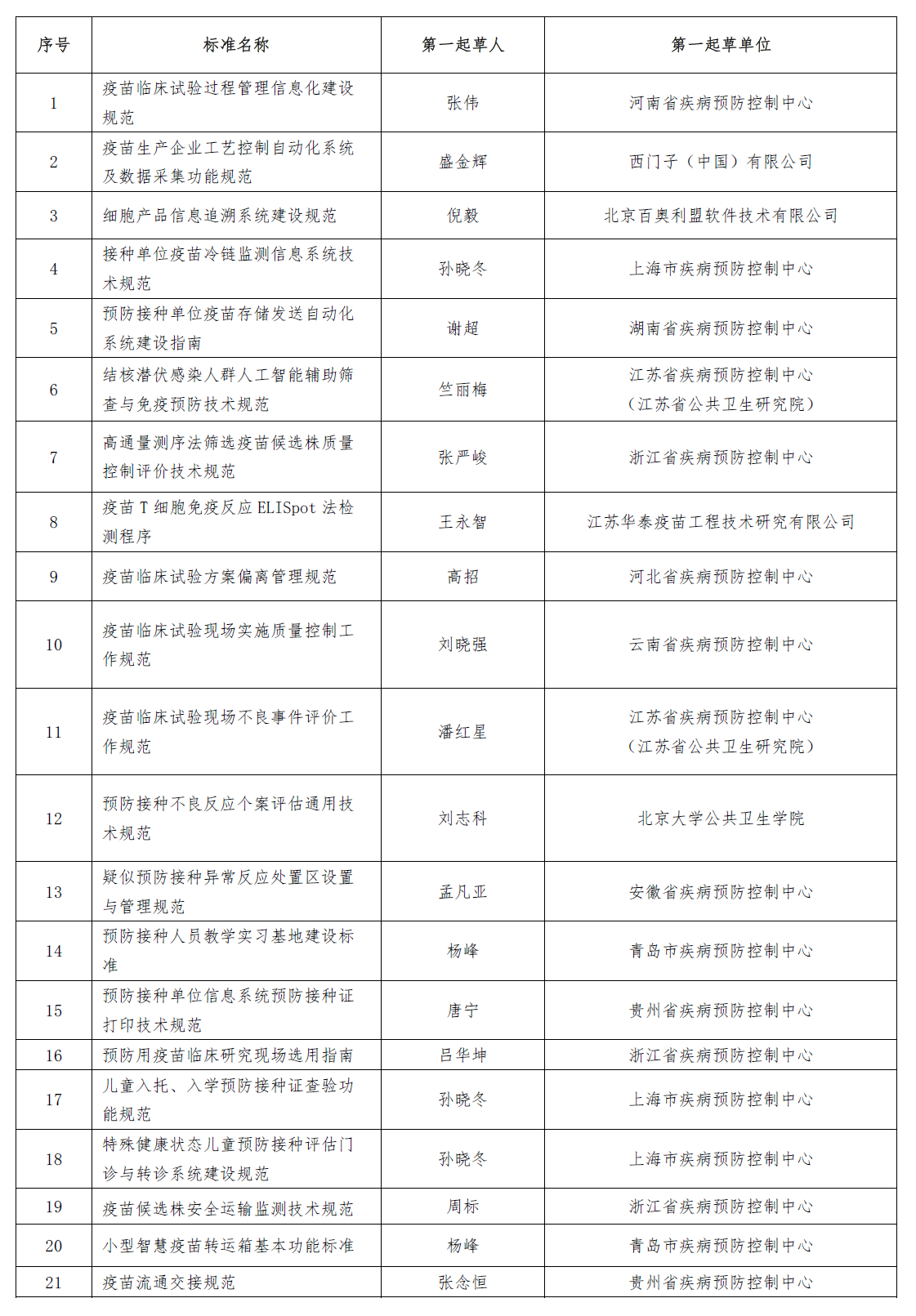
附件 2024年中国疫苗行业协会标准立项清单
 京公网安备 11010102006196号
京公网安备 11010102006196号
